- الهدف من التجربة :
معرفة الروابط في المركبات التساهمية.
- المواد والأدوات المستخدمة :
- مجموعة نماذج الجزيئات (الكرات والوصلات)
- خطوات العمل :
- أُلاحظ الجدول الآتي، ثم أستنتج عدد الروابط التي يمكن أن تكونها كل ذرة منها، وأختار نموذجًا لكل ذرة يتوافق عدد الثقوب فيها مع عدد الروابط، ثم أُدونها في جدول كتاب الأنشطة والتجارب العملية.
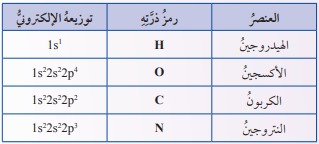
- أُصمم نماذج لكل من الجزيئات الآتية، مستخدمًا مجموعة نماذج الجزيئات (الكرات، والوصلات) كما هو موضح في الأشكال الظاهرة :
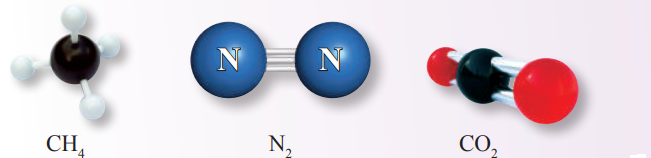
- التحليل والإستنتاج:
1. ما عدد الروابط التي تكونها كل من الذرات : C, O, H, N
2. أستنتج عدد أزواج الإلكترونات المشتركة في الروابط الآتية : ( H – C) ، (O = C)،
3. ما عدد الإلكترونات التي تشارك فيها كل من الذرات السابقة :
4. أستنتج المقصود بالرابطة التساهمية:
- الملاحظات على التجربة :
|
الذرات |
عدد إلكترونات المستوى الخارجي (التكافؤ) |
عدد الروابط التي تكونها الذرة |
عدد أزواج الإلكترونات المشتركة في الرابطة |
عدد الإلكترونات التي تشارك بها الذرة |
|
C |
4 |
4 |
1 : ( H – C) |
4 |
|
O |
2 |
2 |
2 : (O = C) |
2 |
|
H |
1 |
1 |
3 : |
1 |
|
N |
3 |
3 |
|
3 |
الرابطة التساهمية: هي الرابطة الكيميائية الناتجة من تشارك زوج أو أكثر من الإلكترونات بين ذرتين أو أكثر من العناصر اللافلزية