|
أستكشف: الفلزات واللافلزات المواد والأدوات: صفيحة نحاس، صفيحة خارصين، مسحوق كبريت، قطعة كربون، مطرقة، قفافيز. خطوات العمل: أجمع بياناتي: أنشئ جدولا مكونا من ثلاثة أعمدة، عنوان الأول "اسم العنصر"، والثاني "اللمعان" والثالث "قابليته للطرق". 1- ألاحظ: أتفحص لمعان كل عنصر، أي منهما لامع؟ أسجل ملاحظاتي في الجدول. 2- أجرب: أستخدم المطرقة، وأطرق كل عنصر مرات عدة، أي منها قابلة للطرق دون أن تتكسر أو تتفتت؟ أسجل ملاحظاتي في الجدول.
3- أحدد العناصر الصلبة اللامعة والقابلة للطرق. النحاس والخارصين 4- أحدد العناصر غير اللامعة والهشة. الكبريت والكربون 5- أصنف العناصر الواردة في الجدول إلى فلزات لامعة وقابلة للطرق، ولا فلزات هشة غير لامعة.
6- أقارن بين الفلزات واللافلزات؟ الفلزات: عناصر صلبة، لامعة، قابلة للطرق والسحب، وجيدة التوصيل للكهرباء والحرارة. اللافزات: عناصر صلبة أو سائلة أو غازية، غير لامعة، وغير قابلة للطرق والسحب، رديئة التوصيل الحراري والكهربائي. 7- أستنتج مم تتكون العناصر التي درستها؟ |
الذرات
تتنوع المواد من حولنا وتختلف في خصائصها، إذ تتكون من عناصر مختلفة.
وتعد الذرة Atom أصغر جزء من العنصر تكسبه خصائصه التي تميزه عن غيره من العناصر.
والذرات جسيمات متناهية في الصغر لا يمكننا رؤيتها بالمجهر الضوئي المركب، إلا أن هناك مجاهر خاصة أكثر تعقيدا تمكننا من رؤية ترتيبها.
أنظر الشكل الآتي الذي يمثل مجهر ذري يظهر ترتيب ذرات مادة.

تتكون الذرة من ثلاثة أنواع من الجسيمات، هي:
- البروتونات
- النيوترونات
- الإلكترونات
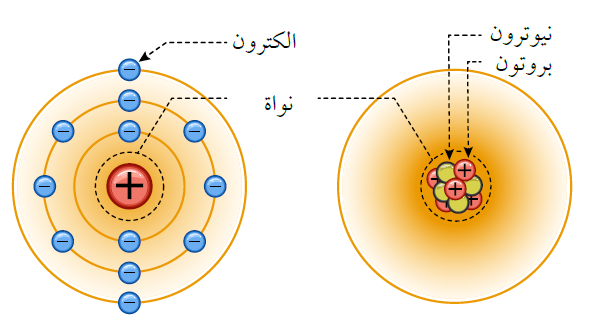
اتفق العلماء على تمثيل نموذج الذرة بشكل كروي، كالآتي:
- مركزه نواة تحتوي على: البروتونات، وهي جسيمات موجبة الشحنة، والنيوترونات: وهي جسيمات شحنتها متعادلة.
- تدور حول النواة: الإلكترونات: هي جسيمات سالبة الشحنة تدور حول نواة الذرة.
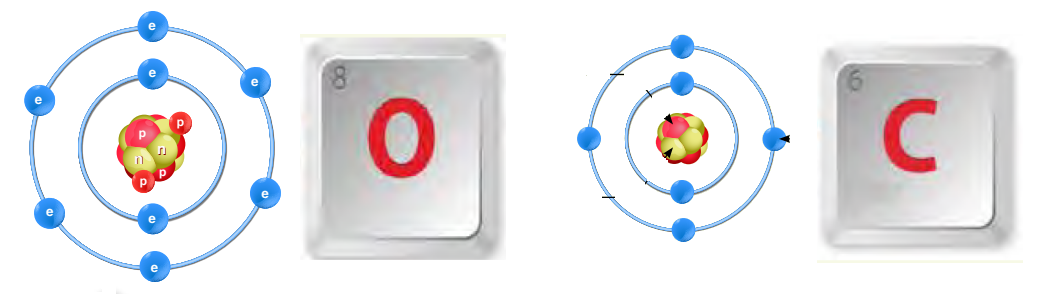
يحدد عدد البروتونات هوية العنصر عن غيره من العناصر، فمثلا:
- تحتوي ذرة الكربون على ستة بروتونات في نواتها.
- تحتوي ذرة الأكسجين على ثمانية بروتونات في نواتها.
ولا يوجد عنصران تحوي ذراتهما العدد نفسه من البروتونات.
ويمثل الشكل الآتي تشابه الذرات في مكوناتها.
|
أتأمل الشكل
أحدد أوجه الشبه والاختلاف في الجسيمات المكونة لكل من ذرة الكربون وذرة الأكسجين. أوجه الشبه: تتكون كل من ذرة الكربون وذرة الأكسجين من الجسيمات نفسها وهي: البروتونات، النيوترونات والإلكترونات. أوجه الاختلاف: تختلف في عدد كل من البروتونات والنيوترونات والإلكترونات: ذرة الأكسجين تحتوي على 8 بروتونات، و8 نيوترونات و8 إلكترونات ذرة الكربون تحتوي على 6 بروتونات و6 نيوترونات و6 إلكترونات. |
ترتيب الذرات
تترتب ذرات عناصر المواد المختلفة بأشكال معينة، فيؤثر ذلك في خصائصها واستخداماتها.
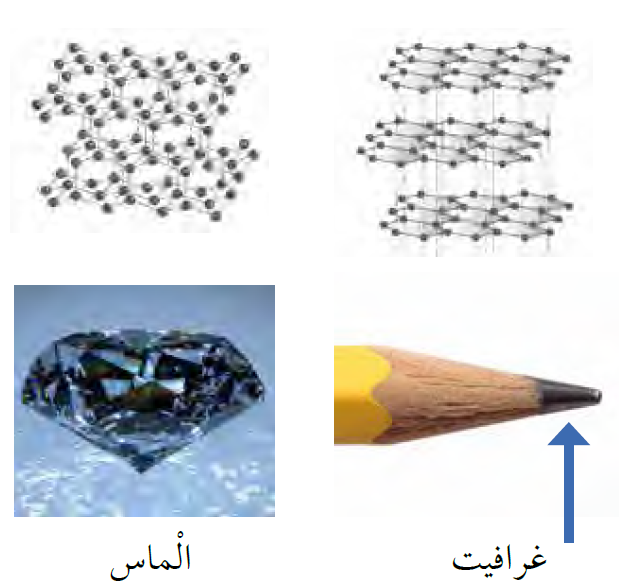
الغرافيت والماس يتكونان من ذرات الكربون إلا أن لهما استخدامات مختلفة، ويعود ذلك إلى طريقة ترتيب ذرات الكربون المكونة لكل منهما.
- عند ترتيب الذرات على شكل طبقات متوازية، فإنها تكون مادة الغرافيت اللينة سهلة الكسر ذات اللون الأسود المستخدمة في صناعة أقلام الرصاص.
- عند ترتيب الذرات على شكل رباعي الأوجه فإنها تكون الماس، الذي يعد من أكثر المعادن قساوة، ويستخدم في صناعة الحلي والمجوهرات.
|
نشاط: ترتيب الذرات المواد والأدوات: قطع معجون ذات لون واحد، ورق أبيض، أقلام ألوان، أعواد تنظيف الأسنان الخشبية. خطوات العمل: 1- أشكل من المعجون (10) كرات صغيرة ومتماثلة في الحجم. تختلف العناصر في ترتيب الذرات وأعدادها. 5- أتواصل: أناقش زملائي في النتائج التي توصلت إليها. |
أتحقق: أقارن بين ذرات الغرافيت والماس من حيث نوعها وترتيبها.
نوع ذرات الماس وذرات الغرافيت نفسها وهي ذرات الكربون وتختلف في طريقة ترتيبها، الغرافيت طبقات متوازية والماس رباعي الأوجه.
الجزيئات
العنصر : مادة نقية تتكون من نوع واحد من الذرات لا يمكن تجزئتها إلى مواد أبسط منها بالطرائق الكيميائية أو الفيزيائية البسيطة، إذ توجد بعض العناصر على شكل ذرات منفردة، مثل الذهب (Au) والألمنيوم (Al) ، وبعضها يوجد على شكل جزيئات.
الجزيء Molecule: يتكون من اتحاد ذرتين أو أكثر من النوع نفسه أو من أنواع ذرات مختلفة من خلال مشاركة الإلكترونات، لذلك قد يكون الجزيء عنصرا أو مركبا.

ويعبر عن الجزيء برمز يدل على أنواع الذرات المكونة له ورقم يدل على عدد كل منها، مثل:
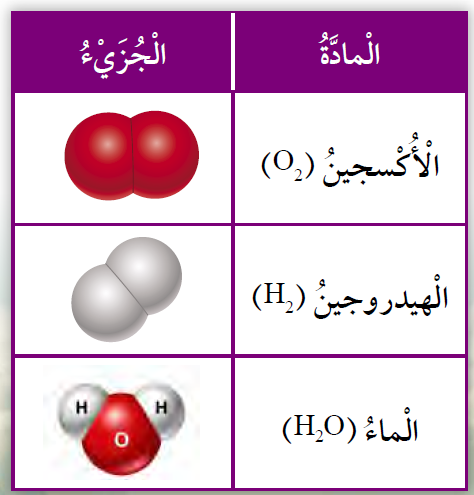
- جزيء الأكسجين (O2) الذي يتكون من اتحاد ذرتي أكسجين.
- جزيء الهيدروجين (H₂) الذي يتكون من اتحاد ذرتي هيدروجين.
وعند اتحاد ذرتين من الهيدروجين مع ذرة أكسجين يتكون جزيء الماء (H2O)، أما إذا اتحدت ذرتا أكسجين مع ذرة كربون فيتكون جزيء ثاني أكسيد الكربون (CO2).
وتختلف جزيئات المواد باختلاف:
- عدد الذرات المكونة له
-نوعها.
أتأمل الجدول الآتي الذي يبين جزيئات مواد مختلفة.